Соли — это сложные вещества, состоящие из ионов металлов и кислотных остатков.
Как видно из определения, соли по составу похожи на кислоты, только вместо атомов водорода они содержат ионы металла. Поэтому их можно также назвать продуктами замещения атомов водорода в кислоте на ионы металла. Например, всем известная поваренная соль NaCl может быть рассмотрена как продукт замещения водорода в соляной кислоте НСl на ион натрия.
Заряд иона натрия 1+, а заряд иона хлора 1-. Так как соединение электронейтрально, формула поваренной соли Na+Cl-. Если же надо вывести формулу сульфида алюминия (III), поступают следующим образом.
- Обозначают заряды ионов, из которых состоит соединение: Al3+S2-. Заряд иона алюминия 3+, а заряд иона серы можно определить по формуле соответствующей сероводородной кислоты H2S, он равен 2-.
- Находят наименьшее общее кратное числовых значений зарядов ионов алюминия и серы (3 и 2), оно равно 6.
- Находят индексы, разделив наименьшее общее кратное на величины зарядов, и записывают формулу:

Аналогично выводят формулы солей кислородсодержащих кислот, имеющих сложные ионы. Выведем, например, формулу кальциевой соли фосфорной кислоты — фосфата кальция. По таблице Менделеева определим заряд иона кальция как элемента главной подгруппы II группы (IIA группы): 2+. По формуле фосфорной кислоты Н3РO4 определим заряд иона, образованного кислотным остатком:![]() Отсюда формула фосфата кальция имеет вид
Отсюда формула фосфата кальция имеет вид
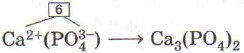
читают «кальций три, пэ-о-четыре дважды»).
Нетрудно заметить, что при выведении формул солей по зарядам ионов вы должны действовать так же, как при выведении формул бинарных соединений по валентности и по степеням окисления образующих их элементов.
Как образуют названия солей бескислородных кислот, вы уже рассмотрели, когда знакомились с номенклатурой бинарных соединений: соли НСl называют хлоридами, а соли H2S — сульфидами.
Названия солей кислородсодержащих кислот составляют из двух слов: названия иона, образованного кислотным остатком, в именительном падеже и названия иона металла — в родительном. Названия ионов кислотных остатков составляют, в свою очередь, из корней названий элементов, с суффиксами -am для высшей степени окисления и -ит для низшей степени окисления атомов элемента-неметалла, образующего сложный ион остатка кислородсодержащей кислоты. Например, соли азотной кислоты HNO3 называют нитратами: KNO3 — нитрат калия, а соли азотистой кислоты HNO2 — нитритами: Ca(NO2)2 — нитрит кальция. Если же металл проявляет различные степени окисления, то их указывают в скобках римской цифрой, например: Fe2+SO3 — сульфит железа (II) и ![]() — сульфат железа (III).
— сульфат железа (III).
Номенклатура солей приведена в таблице.
Номенклатура солей
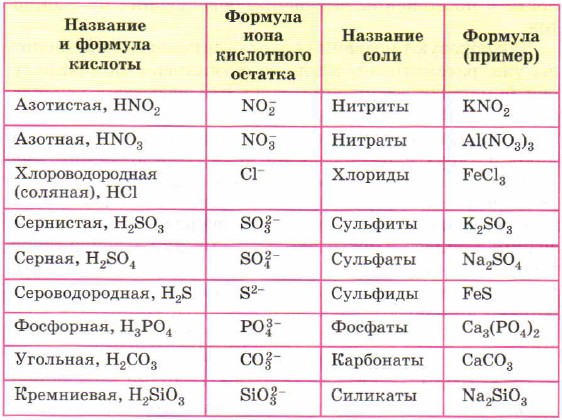
По растворимости в воде соли делят на растворимые (Р), нерастворимые (Н) и малорастворимые (М). Для определения растворимости солей используют таблицу растворимости кислот, оснований и солей в воде. Если под рукой нет этой таблицы, можно воспользоваться приведёнными ниже правилами. Их легко запомнить.
- Растворимы все соли азотной кислоты — нитраты.
- Растворимы все соли соляной кислоты — хлориды, кроме AgCl (Н), РЬСl2 (М).
- Растворимы все соли серной кислоты — сульфаты, кроме BaSO4 (Н), PbSO4 (Н), CaSO4 (М), Ag2SO4 (М).
- Растворимы соли натрия и калия.
- Не растворяются все фосфаты, карбонаты, силикаты и сульфиды, кроме этих солей для Na+ и К+.
Рассмотрим растворимую натриевую соль бескислородной соляной кислоты — хлорид натрия NaCl и нерастворимые кальциевые соли угольной и фосфорной кислот — карбонат кальция СаСO3 и фосфат кальция Са3(РO4)2.
Лабораторный опыт № 12
Ознакомление с коллекцией солей
- Ознакомьтесь с коллекцией выданных вам образцов солей. Запишите их формулы, охарактеризуйте физические свойства, в том числе и растворимость в воде. Рассчитайте молекулярные (молярные) массы солей, а также массовые доли образующих их элементов. Найдите массу 2 моль каждой соли.
Хлорид натрия NaCl — хорошо растворимая в воде соль, известна под названием поваренная соль. Без этой соли невозможна жизнь растений, животных и человека, так как она обеспечивает важнейшие физиологические процессы в организмах: в крови соль создаёт необходимые условия для существования красных кровяных телец, в мышцах обусловливает способность к возбудимости, в желудке образует соляную кислоту, без которой было бы невозможным переваривание и усвоение пищи. Необходимость соли для жизни была известна со времён глубочайшей древности. Значение соли отражено в многочисленных пословицах, поговорках, обычаях. «Хлеб да соль» — вот одно из пожеланий, которым русские люди с давних пор обменивались друг с другом во время приёма пищи, подчёркивая равноценное с хлебом значение соли. Хлеб и соль стали символом гостеприимства и радушия русской нации.
Говорят: «Чтобы узнать человека, надо с ним пуд соли съесть». Оказывается, ждать не так уж долго: за два года двое съедают пуд соли (16 кг), так как в год каждый человек с пищей потребляет от 3 до 5,5 кг соли.
В названиях многих городов и посёлков разных стран присутствует слово соль: Соликамск, Соль-Илецк, Усолье, Усолье-Сибирское, Солт-Лейк-Сити, Солтвиль, Зальцбург и т. д.
Соль образует мощные отложения в земной коре. В Соль-Илецке, например, толщина пласта соли превышает полтора километра. Соли, находящейся в озере Баскунчак в Астраханской области, хватит нашей стране на 400 лет. Огромные количества соли содержат в себе воды морей и океанов. Солью, извлечённой из Мирового океана, можно было бы засыпать всю сушу земного шара слоем в 130 м. Во многих странах Азии и Африки соль добывают из соляных озёр (рис. 66, а), а в европейских странах — часто из соляных шахт (рис. 66, б).

Рис. 66.
Добыча соли:
а — из соляных озёр; б — из шахт
Хлорид натрия широко используют в химической промышленности для получения натрия, хлора, соляной кислоты, в медицине, для приготовления пищи, для консервирования продуктов питания (соление и квашение овощей) и т. д.
Карбонат кальция СаСO3 — нерастворимая в воде соль, из которой многочисленные морские животные (моллюски, раки, простейшие) строят покровы своего тела — раковины (рис. 67) и кораллы.

Рис. 67.
Эти красивые раковины состоят преимущественно из карбоната кальция
Остатки коралловых полипов, с которыми вы познакомились на уроках биологии, образуют тропические острова (атоллы) и коралловые рифы (рис. 68). Наиболее известен Большой Барьерный риф в Австралии. Скапливаясь после гибели своих «хозяев» на дне водоёмов и главным образом морей, эти раковины за десятки и сотни миллионов лет сформировали мощные пласты соединений кальция, давших начало образованию горных пород — известняков СаСO3.
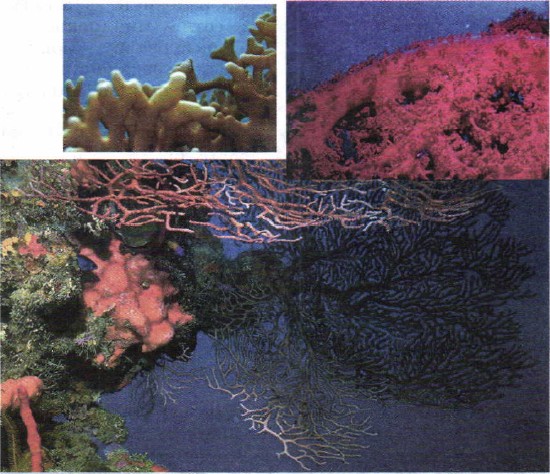
Рис. 68.
Красивейшие морские организмы — кораллы — строят свой скелет из карбоната кальция. Остатки их образуют коралловые атоллы и рифы
Эту же формулу имеет и строительный камень — мрамор, и столь привычный каждому стоящему у доски школьнику мел, который добывают из карьеров или меловых гор (рис. 69). Из известняка получают негашёную и гашёную известь, его применяют в строительстве. Мрамор идёт на изготовление статуй, им отделаны станции метро.

Рис. 69.
Меловые горы
Из карбоната кальция наземные животные «строят» свои скелеты — внутреннюю опору для мягких тканей, которые в десятки раз превышают вес самой опоры.
Фосфат кальция Са3(РO4)2, нерастворимый в воде, — это основа минералов фосфоритов и апатитов. Из них производят фосфорные удобрения, без которых было бы невозможно получение высоких урожаев в сельском хозяйстве. Фосфат кальция также входит в состав костей животных.

